Une étude montre comment une respiration lente induit la tranquillité
Les scientifiques de Stanford ont identifié un petit groupe de neurones qui communiquent ce qui se passe dans le centre de contrôle respiratoire du cerveau à la structure responsable de la génération de l’excitation dans tout le cerveau.

Essayez-le.
Respirez lentement et doucement.
Un sentiment omniprésent de calme descend.
Maintenant, respirez rapidement et frénétiquement. Vous montez en tension.
Pourquoi ?
C’est une question à laquelle la science n’a jamais répondu jusqu’à présent.
Dans une nouvelle étude, des chercheurs de la Stanford University School of Medicine et leurs collègues ont identifié une poignée de cellules nerveuses dans le tronc cérébral qui relient la respiration aux états d’esprit.
Un article décrivant les résultats a été publié le 31 mars 2017 dans Science . Mark Krasnow, MD, PhD, professeur de biochimie, est l’auteur principal. L’autre auteur principal est l’ancien étudiant diplômé de Stanford, Kevin Yackle, MD, PhD, maintenant membre du corps professoral de l’Université de Californie à San Francisco.
Les médecins prescrivent parfois des exercices de contrôle de la respiration aux personnes souffrant de troubles de stress. De même, la pratique du pranayama – contrôler la respiration afin de faire passer sa conscience d’un état excité ou même frénétique à un état plus méditatif – est un élément central de pratiquement toutes les variétés de yoga.
« Cette étude est intrigante car elle fournit une compréhension cellulaire et moléculaire de la façon dont cela pourrait fonctionner », a déclaré Krasnow.
Minuscule amas de neurones
Le minuscule groupe de neurones reliant la respiration à la relaxation, l’attention, l’excitation et l’anxiété est situé profondément dans le tronc cérébral. Ce cluster, situé dans une zone que Krasnow appelle le stimulateur cardiaque pour la respiration, a été découvert chez la souris par le co-auteur de l’étude Jack Feldman , PhD, professeur de neurobiologie à l’UCLA, qui a publié ses découvertes en 1991. Une structure équivalente a depuis été identifiée dans humains.
« Le stimulateur respiratoire a, à certains égards, un travail plus difficile que son homologue dans le cœur », a déclaré Krasnow, qui est également chercheur à l’Institut médical Howard Hughes . « Contrairement au continuum unidimensionnel, lent à rapide, du cœur, il existe de nombreux types distincts de respirations : régulières, excitées, soupirant, bâillant, haletant, dormant, riant, sanglotant. Nous nous sommes demandé si différents sous-types de neurones au sein du centre de contrôle respiratoire pourraient être chargés de générer ces différents types de souffle.
Sur cette intuition, Yackle a cherché dans des bases de données publiques pour assembler une liste de gènes qui sont préférentiellement activés dans la partie du tronc cérébral de la souris où réside le centre de contrôle de la respiration. Le terme technique de ce centre est le complexe pré-Bötzinger, ou préBötC.
Il a identifié un certain nombre de ces gènes, permettant aux chercheurs d’identifier plus de 60 sous-types neuronaux distincts, physiquement différenciés les uns des autres par leurs signatures d’activation génique mais se mêlant dans le préBötC comme des brins de spaghetti bien agités. Les scientifiques ont pu utiliser ces gènes, et les produits protéiques dont ils sont les recettes, comme marqueurs permettant de cibler les différents sous-types neuronaux.
Éliminer les neurones
Désormais, les scientifiques pourraient évaluer systématiquement le rôle de chaque sous-population neuronale chez les souris de laboratoire. Grâce à des technologies avancées, ils pourraient détruire sélectivement n’importe lequel de ces sous-types neuronaux – et uniquement ce sous-type – sur la base de sa signature unique de gènes actifs. Ensuite, ils ont pu observer comment la perte de ce sous-type particulier affectait la respiration des animaux. En 2016, en collaboration avec Feldman, ils ont réussi à isoler une sous-population de neurones dans le préBötC qui contrôle explicitement un type de respiration : le soupir. Assommer ces neurones a éliminé les soupirs mais n’a pas affecté les autres modes de respiration. La découverte a été publiée dans Nature en 2016.
Krasnow et Yackle ont ensuite entrepris de découvrir le rôle respiratoire d’une autre sous-population d’environ 175 neurones préBötC se distinguant par leur expression commune de deux marqueurs génétiques appelés Cdh9 et Dbx1. Ils ont bio-conçu des souris dans lesquelles ils pouvaient éliminer, à volonté, les neurones portant ces deux marqueurs.
Mais une fois que ces rongeurs ont eu leurs neurones Cdh9/Dbx1 éliminés, ils ont semblé accepter la perte sans problème. Contrairement à leurs frères privés de soupir, il n’y avait aucune lacune dans le portefeuille de variations respiratoires de ces souris.
« J’ai d’abord été déçu », a déclaré Yackle. Mais quelques jours après, il remarqua quelque chose : pour les souris, les animaux étaient extraordinairement calmes. « Si vous les mettez dans un nouvel environnement, qui stimule normalement beaucoup de reniflement et d’exploration », a déclaré Yackle, « ils resteraient assis à se toiletter » – preuve de ce qui passe pour de la douceur quand vous êtes une souris.
Se détendre
Une analyse plus approfondie a montré que si ces souris affichaient toujours la palette complète des variétés respiratoires, des soupirs aux reniflements, les proportions relatives de ces variétés avaient changé. Il y avait moins de respirations «actives» rapides et «reniflées» plus rapides, et des respirations plus lentes associées à la détente.
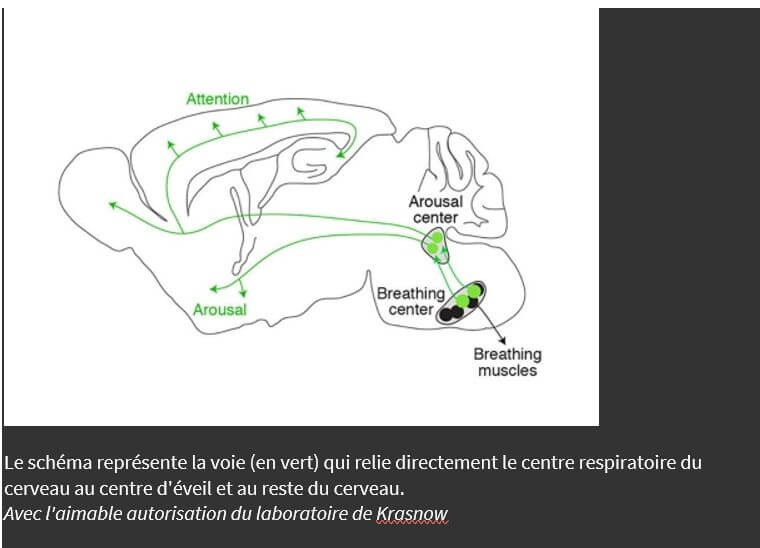
Les chercheurs ont supposé qu’au lieu de réguler la respiration, ces neurones l’espionnaient et rapportaient leur découverte à une autre structure du tronc cérébral. Cette structure, le locus coeruleus, envoie des projections à pratiquement toutes les parties du cerveau et provoque l’éveil : nous réveille du sommeil, maintient notre vigilance et, si elle est excessive, déclenche l’anxiété et la détresse. On sait que les neurones du locus coeruleus présentent un comportement rythmique dont le rythme est corrélé à celui de la respiration. Dans une série d’expériences, les chercheurs de Stanford ont prouvé que les neurones préBötC qui expriment Cadh9 et Dbx1 se projettent non seulement sur le locus coeruleus – une nouvelle découverte – mais activent ses projections à longue distance, favorisant l’excitation cérébrale.
« Si quelque chose altère ou accélère votre respiration, vous devez le savoir immédiatement », a déclaré Krasnow. « Ces 175 neurones, qui informent le reste du cerveau de ce qui se passe, sont absolument essentiels. » « Le preBötC semble maintenant jouer un rôle clé dans les effets de la respiration sur l’excitation et l’émotion, comme on le voit pendant la méditation », a déclaré Feldman. « Nous espérons que la compréhension de la fonction de ce centre conduira à des thérapies contre le stress, la dépression et d’autres émotions négatives. »
Les autres co-auteurs de Stanford sont John Huguenard , PhD, professeur de neurologie et de sciences neurologiques ; Liqun Luo , PhD, professeur de biologie et chercheur HHMI; l’ancienne chercheuse postdoctorale Lindsay Schwarz, PhD; et l’étudiant diplômé Jordan Sorkin.
Un chercheur de la Chicago Medical School est également co-auteur de l’étude.
Krasnow est également directeur exécutif du Wall Center for Pulmonary Vascular Disease , membre de l’Institut des neurosciences de Stanford , de l’Institut cardiovasculaire , de l’Institut du cancer et de Bio-X .
L’étude a été financée par les National Institutes of Health (subventions HL70029 et HL40959) et HHMI .
Le département de biochimie de Stanford a également soutenu le travail.
Bruce Goldman est rédacteur scientifique principal au Bureau des communications.
Présentation de l’Etude
PMCID : PMC5505554
ID NIHMS : NIHMS869084
PMID : 28360327
Neurones du centre de contrôle de la respiration qui favorisent l’excitation chez les souris
Kevin Yackle , 1, # Lindsay A. Schwarz , 2 Kaiwen Kam , 3, 4 Jordan M. Sorokin , 5 John R. Huguenard , 5 Jack L. Feldman , 3 Liqun Luo , 2 et Mark A. Krasnow 1, *
Données associées
La respiration lente et contrôlée est utilisée depuis des siècles pour favoriser l’apaisement mental, et elle est utilisée en clinique pour supprimer l’excitation excessive telle que les attaques de panique. Cependant, la base physiologique et neurale de la relation entre la respiration et l’activité cérébrale d’ordre supérieur est inconnue. Nous avons trouvé une sous-population neuronale dans le complexe preBötzinger de la souris (preBötC), le principal générateur de rythme respiratoire, qui régule l’équilibre entre les comportements calmes et d’éveil. Ablation génétique conditionnelle et bilatérale de ~175 Cdh9/Dbx1les neurones préBötC doublement positifs chez les souris adultes ont laissé la respiration intacte mais ont augmenté les comportements calmes et ont diminué le temps dans les états d’éveil. Ces neurones se projettent, synapsent et régulent positivement les neurones noradrénergiques dans le locus coeruleus, un centre cérébral impliqué dans l’attention, l’éveil et la panique qui se projette dans tout le cerveau.
Bien que la respiration soit généralement considérée comme une fonction autonome simple qui maintient la vie, on sait depuis longtemps qu’elle influence le comportement et la pensée d’ordre supérieur ( 1 ). La respiration lente contrôlée est utilisée par les praticiens du pranayama yoga et d’autres formes de méditation pour favoriser l’apaisement mental et les états contemplatifs, et elle est utilisée cliniquement pour supprimer l’excitation et le stress excessifs tels que certains types d’attaques de panique (2 , 3 ) . Alors que l’effet de la respiration sur le comportement et l’état mental pourrait facilement être indirect, il pourrait également y avoir des connexions plus directes et un impact du centre respiratoire sur la fonction cérébrale d’ordre supérieur ( 4 ), comme démontré ici.
Le complexe preBötzinger (preBötC) est un groupe de plusieurs milliers de neurones dans la moelle ventrolatérale du cerveau murin qui peut générer de manière autonome des rythmes respiratoires dans des tranches de cerveau explantées ( 5 , 6 ), et dont l’activité rythmique in vivo initie la respiration en activant de façon récurrente la pré- motoneurones et motoneurones des muscles respiratoires ( 5 ). Le preBötC n’est pas une population homogène de neurones mais est composé de sous-populations neuronales distinctes mais entremêlées ( 5 , 7 ), dont l’une est essentielle pour la génération du rythme respiratoire ( 8 , 9 ) et une autre pour le soupir ( 10 ).
Pour explorer systématiquement la diversité moléculaire des neurones du centre respiratoire, nous avons criblé les modèles d’expression de plus de 19 000 gènes dans la base de données du cerveau postérieur de la souris Euroexpress e14.5 ( 7 , 11 ). La cadhérine-9 (Cdh9) était le gène le plus sélectivement exprimé dans preBötC (Figure 1A). Nous avons construit un transgène de chromosome artificiel bactérien (BAC) avec une séquence codante mOrange insérée au niveau du codon d’initiation de la traduction Cdh9 (Figure 1B). Le nombre de cellules dans les cerveaux postnatals précoces a détecté 319 ± 130 (n = 6) cellules exprimant Cdh9-mOrange dans preBötC (Figure 1C). Ces cellules se sont mêlées à des neurones exprimant des marqueurs canoniques préBötC Somatostatine (SST) et Neurokinine 1 (NK1R) (Fig. 1D à E, et fig. S1A–E ). Peu exprimaient les marqueurs eux-mêmes : 0 des 43 cellules Cdh9+ notées étaient SST+, et 7 des 179 cellules Cdh9+ notées (4 %) étaient NK1R+. Toutes les cellules exprimant Cdh9-mOrange co-expriment le marqueur neuronal NeuN (n = 61 cellules,Figure 1F). Ces neurones exprimant Cdh9-mOrange peuvent être divisés en sept sous-types basés sur l’expression différentielle des facteurs de transcription PAX2, DACH1, LMO4, EVX1 et Dbx1 (7 ) . Nous nous sommes concentrés sur les ~175 neurones de chaque préBötC ( fig. S1F–J ; ~350 neurones bilatéralement) qui co-expriment le marqueur de lignée Dbx1, la sous-population principale (56 %, 165 des 292 cellules Cdh9+ notées, étaient Dbx1-LacZ+) on appelle les neurones Cdh9/Dbx1 (Fig. 1G à I).
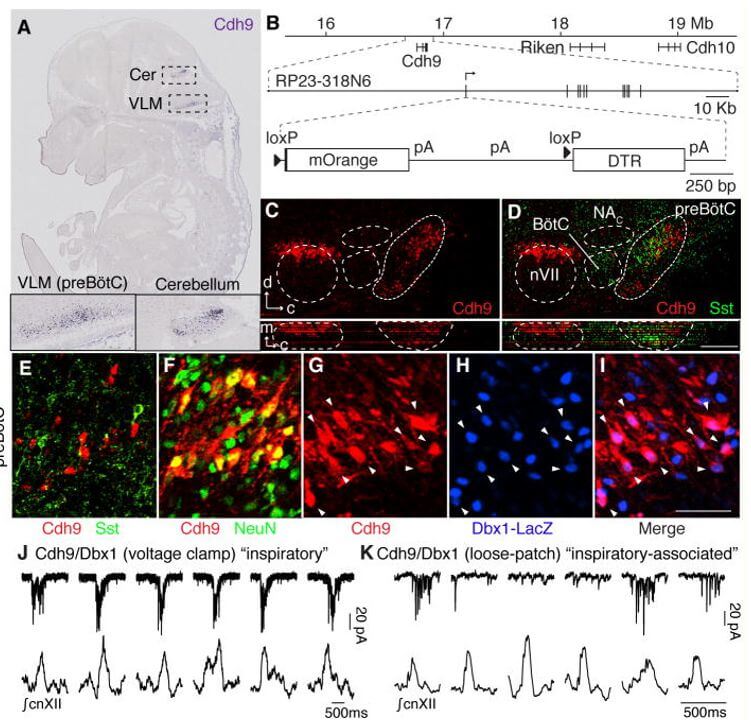
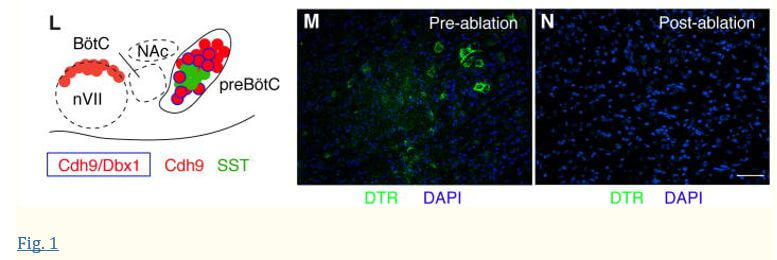
Identification et ablation génétique des neurones doublement positifs Cdh9/Dbx1 dans le préBötC
A , expression de l’ARNm de Cdh9 (bleu) dans la section de l’embryon de souris E14.5 ( 11 ). Encarts, médullaire ventrolatérale, cervelet ventral. B , (Haut) locus Cdh9 sur le chromosome 15 (nombres, distance du centromère). (Moyen) BAC RP23-318N6. Lignes verticales, exons Cdh9 . (En bas) Transgène Cdh9-LOSL-DTR BAC : insertion au niveau du codon d’initiation Cdh9 de la séquence mOrange et des signaux de polyadénylation (pA), flanqués de sites loxP (triangles), suivis de la séquence DTR. CD, Sections de la moelle ventrolatérale de souris P0 Cdh9-LOSL-DTR immunocolorées pour mOrange pour montrer l’expression de Cdh9 (rouge) et souris de type sauvage P0 immunocolorées pour la somatostatine (SST, vert), montrées alignées (enregistrées par le noyau compact ambigu (NA C ) , crânien nerf 7 (nVII) et surface ventrale du tronc cérébral) dans le plan sagittal (supérieur) et en projection transversale (panneaux inférieurs). d, dorsale ; c, caudale ; m, médial. Barre, 200 μm. E–I, preBötC de P0 Cdh9 LOSL-DTR (E,F) ou Cdh9-LOSL-DTR; Souris Dbx1-lacZ (G–I) immunocolorée pour Cdh9-mOrange (E–G,I, rouge), SST (E , vert), NeuN (F, vert) ou bêta-galactosidase (Dbx1-LacZ, H,I, bleu). Parmi les neurones Cdh9, aucun ne co-exprimait SST (n = 43 cellules), tous co-exprimaient NeuN (n = 57) et 56 % co-exprimaient le journaliste Dbx1 (n = 292, têtes de flèche). Barre (pour E – I), 50 μm. J, K,Enregistrements de tension de cellules entières (en haut, pA, picoAmp) de neurones Cdh9/Dbx1 preBötC dans des préparations de tranches (en haut) et activité cnXII intégrée simultanée (en bas). Le neurone en J (neurone 1, tableau S1 ) montre des sursauts dans tous les événements inspiratoires (« schéma inspiratoire »). Le neurone en K (neurone 3) montre une activité plus étendue mais n’éclate que lors de certains événements (« associés à l’inspiration »). Barres, 500 ms. L , Schéma de la moelle ventrolatérale. Les neurones Cdh9/Dbx1 (bordure bleue) se mélangent avec SST (vert) et d’autres neurones Cdh9 (rouge) dans preBötC. M, N , Marquage génétique intersectionnel des neurones Cdh9/Dbx1 preBötC avec DTR (immunocoloration, vert) chez ~ P35 souris Cdh9-LOSL-DTR; Dbx1-cre avant (M) et après (N) injection intrapéritonéale de DT pour les enlever. Barre, 50 μm.
Nous avons enregistré électrophysiologiquement 26 neurones mOrange-positifs dans 15 préparations de tranches préBötC de Cdh9-mOrange; Dbx1-lacZ double souris transgéniques P0–5, puis post-colorées pour la bêta-galactosidase (lacZ) dans certaines préparations pour identifier les enregistrements de neurones Cdh9/Dbx1 ( tableau S1 ). Nous avons définitivement identifié cinq neurones Cdh9/Dbx1. L’un a montré des bouffées de potentiels d’action juste avant ou pendant chaque bouffée inspiratoire préBötC (Fig. 1J, et fig. S2 ), comme la plupart des autres neurones préBötC de la lignée Dbx1 ( 12 ). Trois autres neurones étaient plus largement actifs avec des rafales pendant certaines mais pas toutes les rafales inspiratoires préBötC (42, 41 et 88 % des rafales inspiratoires,Figure 1K, et fig. S2 ), appelé modèle d’activité « associé à l’inspiration ». L’autre neurone a montré une activité sporadique sans relation apparente avec les bouffées inspiratoires pré-BötC. Sept des 15 neurones Cdh9-mOrange dont le statut d’expression de Dbx1-lacZ n’a pas été déterminé présentaient également des schémas inspiratoires (4 neurones) ou associés à l’inspiration (2 neurones) ( tableau S1 ).
Nous avons utilisé la génétique intersectionnelle (Cdh9-LOSL-DTR;Dbx1-Cre) (Fig. 1B, M, N) pour exprimer le récepteur de la toxine diphtérique humaine (DTR) uniquement dans les cellules de la lignée Dbx1 qui co-expriment Cdh9, de sorte que les neurones Cdh9/Dbx1 pourraient être spécifiquement enlevés par injection intrapéritonéale de toxine diphtérique. Nous nous attendions à ce qu’il y ait peu ou pas de cellules en dehors des neurones préBötC Cdh9/Dbx1 qui expriment les deux gènes ( 11 , 13 ). Nous avons examiné cela de deux manières. Tout d’abord, nous avons comparé l’expression de mOrange chez les souris transgéniques Cdh9-LOSL-DTR et Cdh9-LOSL-DTR;Dbx1-Cre en immunomarquant des coupes en série de cerveaux adultes. Les seules régions où Dbx1-Cre a réduit le nombre de cellules exprimant mOrange étaient préBötC et colliculus inférieur ( fig. S3). La co-coloration avec d’autres marqueurs a montré que la perte de mOrange dans preBötC était spécifique et complète pour les neurones Cdh9/Dbx1 et avait peu ou pas d’effet sur les six autres types de cellules préBötC positives pour Cdh9 (Dbx1-négatif) ( fig. S4 ) . Deuxièmement, l’immunomarquage de coupes en série de cerveaux adultes Cdh9-LOSL-DTR; Dbx1-Cre a détecté l’expression de DTR uniquement dans les neurones préBötC Cdh9 / Dbx1 (Figure 1M) et le colliculus inférieur ( fig. S3 ). L’injection intrapéritonéale de toxine diphtérique une fois par jour pendant trois jours a éliminé les cellules exprimant le DTR (Figure 1N).
Nous avons analysé des souris adultes plusieurs jours après l’ablation des neurones Cdh9/Dbx1. Nous nous attendions à ce que les neurones Cdh9/Dbx1 soient essentiels à la respiration et à la viabilité car les neurones Dbx1 sont essentiels à la respiration in vivo ( 8 , 9 ) et l’ablation de seulement 85 neurones Dbx1 aléatoires abolit les rythmes préBötC in vitro ( 14 ). Cependant, il n’y avait aucun effet manifeste sur la viabilité (3 des 3 souris notées vivantes > 1 an après l’ablation), la respiration ou les comportements sensoriels et moteurs. La pléthysmographie de souris adultes en mouvement libre après ablation n’a pas détecté de différences significatives dans le temps inspiratoire, le temps expiratoire ou le volume courant des respirations standard (eupnéiques) ( figs. S5A, S6 ). Aucune différence n’a été détectée dans les caractéristiques des quatre types de respiration variables ( fig. S5B à E, S6) ou des respirations pendant le sommeil ou dans des conditions hypercapniques ou hypoxiques ( figs. S5F à H, S6 ).
Il y avait, cependant, un changement dans l’abondance des différents types de respiration, d’abord noté dans les histogrammes de la fréquence respiratoire (RR) : l’ablation de Cdh9/Dbx1 a déplacé la distribution vers des respirations plus lentes (faible RR) (Figure 2B). L’inspection des traces du pléthysmographe a indiqué que le changement était dû à une augmentation des respirations lentes (eupnéiques et toilettage) associées à des comportements calmes, et à une réduction des respirations rapides associées au reniflement et à d’autres comportements actifs (Figure 2A, et fig. S7 ).
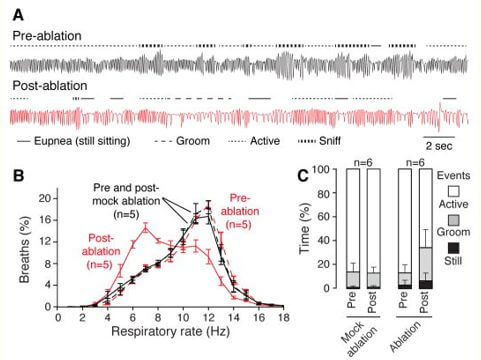
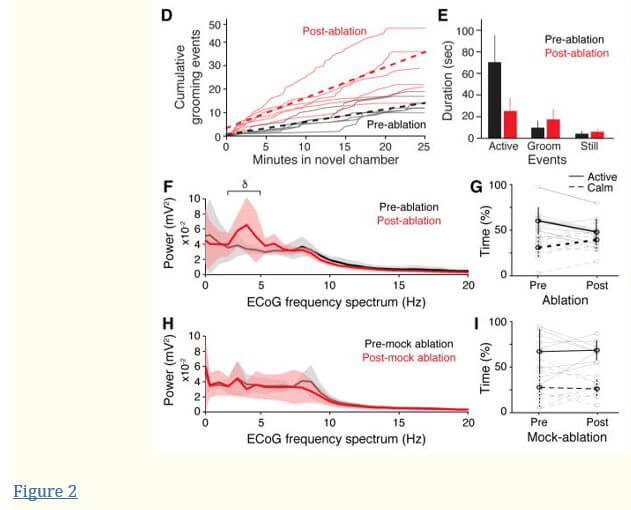
Changements respiratoires et comportementaux après ablation des neurones Cdh9/Dbx1
A , traces de flux d’air de pléthysmographie de souris Cdh9-LOSL-DTR; Dbx1-Cre avant (noir) et 2 jours après (rouge) ablation Cdh9/Dbx1. Notez plus de respirations de toilettage (− −) et eupnéiques (−) et moins de respirations actives (− −) et de reniflement (−−) après l’ablation. Barre, 2 secondes. B, Distribution des fréquences respiratoires (Hz, taille de bac 1 Hz) dans un test de contrôle de 40 minutes (type sauvage, Cdh9-LOSL-DTR ou Dbx1-Cre ; noir, n = 5) et expérimental (Cdh9-LOSL-DTR ; Dbx1 -Cre; rouge, n = 5) animaux avant (lignes pointillées) et 2 jours après (lignes pleines) ablation Cdh9/Dbx1. C, Pourcentage de temps passé dans la chambre de pléthysmographie toujours assis (noir), se toilettant (gris) ou actif (blanc) par des souris témoins (n = 6) ou expérimentales (n = 6) avant (pré) ou 2 jours après (post) ablation ou simulacre d’ablation. Valeur de p comparant le comportement avant et après l’ablation : actif (0,02), toilettage (0,02), toujours assis (0,07). D, Événements de toilettage dans la nouvelle chambre de souris Cdh9-LOSL-DTR; Dbx1-Cre avant (noir) ou après (rouge) ablation. Lignes pleines, souris individuelles (n = 6) ; ligne pointillée, moyenne. E, Durée des comportements en C (moyenne ± SD, n = 6). Après ablation, les épisodes actifs raccourcis (p = 0,005), le toilettage et la position assise montraient une tendance non significative à l’allongement (p = 0,24 et 0,21, respectivement). Analyse spectrale de puissance F, H, ECoG (moyenne (traits pleins) ±SEM) d’enregistrement de 20 minutes (essai 1) de souris Cdh9-LOSL-DTR; Dbx1-Cre (F, n = 5) ou contrôle Cdh9-LOSL-DTR (H, n = 4) avant (noir) ou 4– 10 jours après (rouge) ablation. δ , onde delta. V, tension. Un comportement actif est corrélé à une respiration plus rapide ( fig. S15C–E ). G,I, Temps passé dans des états comportementaux actifs (ligne noire continue, moyenne ± SEM) et calmes (ligne noire pointillée) définis par EMG et ECoG ( fig. S15 ) d’animaux individuels en F,H (lignes grises) pendant deux 20 -dosages minute pré- et post-ablation Cdh9/Dbx1. Notez une diminution active et une augmentation des périodes de calme après l’ablation chez les animaux de laboratoire (p = 0,001 et 0,02, respectivement, test t apparié) et aucun changement chez les témoins (p = 0,86 et 0,81, respectivement).
Le changement des schémas respiratoires après l’ablation neurale Cdh9/Dbx1 s’est accompagné d’un changement de comportement correspondant. L’ablation a réduit l’exploration d’un nouvel environnement (87 % ± 9 % contre 62 % ± 20 % de temps passé en exploration active, avant et après l’ablation ; p = 0,02) et a triplé le temps consacré au toilettage (10 % ± 7 % contre 31 % ± 16 % ; p = 0,02) et toujours assis deux fois (3 % ± 4 % contre 7 % ± 7 % ; p = 0,07), bien que ce dernier n’atteigne pas la signification statistique (Figure 2C). Il y a eu une augmentation du nombre d’épisodes calmes (Figure 2D) et leur durée (Figure 2E, et film S1 ). Étant donné que le schéma respiratoire associé à chaque état comportemental n’a pas été modifié de manière détectable par l’ablation ( fig. S5, S6 ), le changement observé dans la distribution RR pourrait s’expliquer par le changement global de comportement ( fig. S8 ) : un passage d’actif à calme comportements. La surveillance électrocorticographique (ECoG) a montré une augmentation de l’activité cérébrale à ondes lentes (delta, 2–4 Hz) après l’ablation (Figure 2F), et une diminution sélective du temps passé dans un état cérébral actif dominé par l’activité thêta (Figure 2G) par rapport aux témoins de même portée (Figure 2H, je). Ces changements pourraient être temporairement inversés en éclairant la chambre, fournissant un stimulus qui annule apparemment la diminution de l’excitation causée par Cdh9/Dbx1ablation ( fig. S9 ).
Pour confirmer que les changements comportementaux et respiratoires observés étaient dus à l’ablation des neurones dans le préBötC, nous avons limité l’induction DTR et donc l’ablation neurale aux seuls neurones préBötC exprimant Cdh9 ( fig. S10A–C ). Les animaux ont montré une diminution des comportements exploratoires actifs et des schémas respiratoires et une augmentation des comportements calmes et des schémas respiratoires similaires aux animaux avec des neurones Cdh9/Dbx1 enlevés en utilisant notre stratégie génétique intersectionnelle (comparer fig. S10D, E etFigure 2).
La diminution du comportement actif et l’augmentation des ondes delta ECoG observées après l’ablation des neurones Cdh9/Dbx1 rappellent les changements consécutifs au silence ou à l’ablation du locus coeruleus (LC), un noyau noradrénergique du pont impliqué dans l’éveil généralisé, le stress et le sommeil. transitions d’éveil ( 15 ). Nous avons ainsi microinjecté deux traceurs rétrogrades dans le LC et constaté que les deux neurones Cdh9-mOrange marqués dans preBötC (FluorGold : fig. S11A à C; billes rétrogrades fluorescentes : données non présentées). La plupart des neurones préBötC marqués Cdh9-mOrange (85 %, 23/27, n = 40 sections, 3 souris) étaient controlatéraux au site d’injection. La connexion est sélective car la plupart des neurones préBötC marqués exprimaient Cdh9-mOrange (72 %, 13/18, n = 10 sections, 4 souris), et aucun marquage rétrograde des neurones Cdh9-mOrange n’a été observé après injection de traceur dans les régions entourant le LC ( n = 4 injections).
Nous avons testé si la connexion observée entre les neurones préBötC et le LC est directe vers les neurones noradrénergiques (exprimant la dopamine bêta hydroxylase (Dbh)) qui dominent le LC ( 15 ). Injection de virus auxiliaires AAV Cre-dépendants (AAV-FLExLoxP-TVA:mCherry et AAV-FLExLoxP-glycoprotéine de la rage), qui permet l’infection et la propagation monosynaptique d’un virus de la rage pseudotypé envA, à glycoprotéine supprimée et exprimant la GFP (RVdG) ( 16 ), dans le LC de souris Dbh-Cre; Cdh9-mOrange a entraîné une infection spécifique des neurones « starter » LC par RVdG ( fig. S12 ) et un traçage trans-synaptique rétrograde sélectif (marquage GFP) des neurones Cdh9-mOrange dans le préBötC (Figures 3A à Det fig. S11D à F ). Nous avons de nouveau observé un fort biais pour étiqueter le preBötC controlatéral plutôt que ipsilatéral (comparerFigures 3A à Cet fig. S11D à F ). La plupart des neurones marqués à la GFP dans le préBötC controlatéral (63 %, 45/72, n = 18 sections, 3 souris) exprimaient Cdh9-mOrange, alors que peu de neurones préBötC ipsilatéraux marqués exprimaient Cdh9-mOrange (7 %, 7/ 94, n = 18 coupes, 3 souris). Presque tous les neurones exprimant la GFP ipsilatérale étaient situés en dehors de la région canonique préBötC définie par l’expression de la somatostatine, de sorte qu’ils ne sont probablement pas des neurones préBötC ( fig. S13 ). Des expériences de contrôle chez des souris sans Dbh-Cre n’ont pas montré de neurones préBötC doublement positifs ( fig. S12 ).
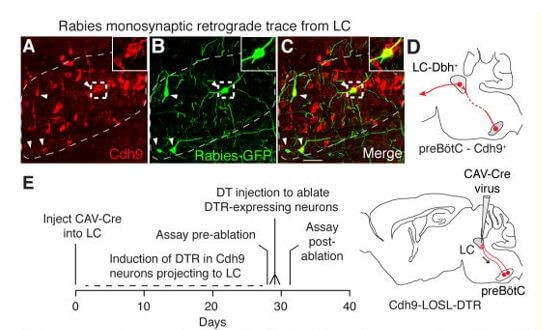
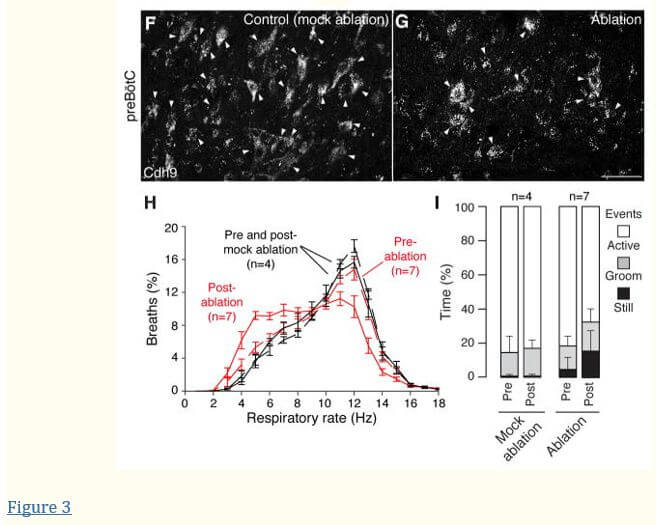
Effet sur la respiration et le comportement de l’ablation des neurones Cdh9 qui se projettent et se synapsent sur les neurones LC
A–D, Trace rétrograde monosynaptique du virus de la rage à partir des neurones du locus coeruleus (LC) exprimant la dopamine bêta hydroxylase (Dbh). Section à travers le préBötC controlatéral (A–C) de la souris adulte Cdh9-LOSL-DTR; Dbh-Cre 5 jours après l’injection unilatérale de LC de la rage-GFP et du virus auxiliaire, immunocolorée pour montrer les neurones Cdh9 (mOrange, rouge). Pointes de flèches, colocalisation de GFP et mOrange. Encarts, régions encadrées. Barre, 50 μm. D , Schéma de la projection monosynaptique (ligne rouge) des neurones Cdh9 preBötC (cercle rouge) au LC controlatéral, qui se projette sur les structures cérébrales supérieures (flèche). E,Schéma d’ablation uniquement des neurones préBötC exprimant Cdh9 qui se projettent vers LC. Le virus CAV-Cre injecté bilatéralement dans le LC de souris adultes Cdh9-LOSL-DTR (à droite) est absorbé par les neurones Cdh9 preBötC qui s’y projettent (rouge). Cre induit l’expression de DTR et l’injection de DT induit l’ablation. F – G, expression preBötC Cdh9-mOrange (blanc) chez des souris Cdh9-LOSL-DTR témoins non injectées (F, simulacre d’ablation) et CAV-Cre injectées (G, ablation) 2 jours après l’injection de DT. Barre, 50 μm. La quantification a montré une réduction de 32 % (moyenne) et de 50 % (maximale) des neurones mOrange (n = 15 sections), proche de la valeur attendue si tous les neurones Cdh9/Dbx1 preBötC (50 % des neurones Cdh9) se projettent sur LC. H , Distribution des fréquences respiratoires dans un test de 40 min (comme dansFigure 2B) de CAV-Cre injecté souris adultes Cdh9-LOSL-DTR (rouge, n = 7) ou compagnons de litière de type sauvage (noir, n = 4) avant (pointillés) et 2 jours après (solide) injection DT. I , Analyse comportementale (comme dansFigure 2C) de souris en H. Valeurs p pré-vs post-ablation : actives (0,015), toilettage (0,37) et toujours assises (0,015). L’augmentation des événements calmes chez les souris expérimentales de pré-ablation par rapport aux souris témoins était reproductible ; cela peut être dû à la toxicité du DTR induite dans les neurones adultes, qui curieusement n’est pas observée chez les souris Cdh9-LOSL-DTR; Dbx1-Cre lorsque le DTR est exprimé au début du développement, peut-être en raison d’une compensation développementale.
Nous avons micro-injecté un virus exprimant Cre transporté de manière rétrograde, l’adénovirus canin de type 2-Cre (CAV-Cre), bilatéralement dans le LC de souris Cdh9-LOSL-DTR pour éliminer mOrange et exprimer DTR uniquement dans les neurones exprimant Cdh9 qui projettent vers CL (Figure 3E). Avant l’injection de DT, les animaux respiraient et se comportaient normalement, bien qu’il y ait eu une augmentation de la respiration calme par rapport aux contrôles fictifs, peut-être en raison de la toxicité neurale associée à l’expression induite de DTR (Figure 3H et moi). 4 à 10 jours après l’injection de DT et l’ablation des neurones préBötC projetant LC et exprimant Cdh9 (Figures 3F, G), il y a eu un changement dans la respiration (Figure 3H) et diminution des comportements actifs (Figure 3I) qui imitaient celles observées après ablation des neurones Cdh9/Dbx1 préBötC (comparer àFigures 2B et C).
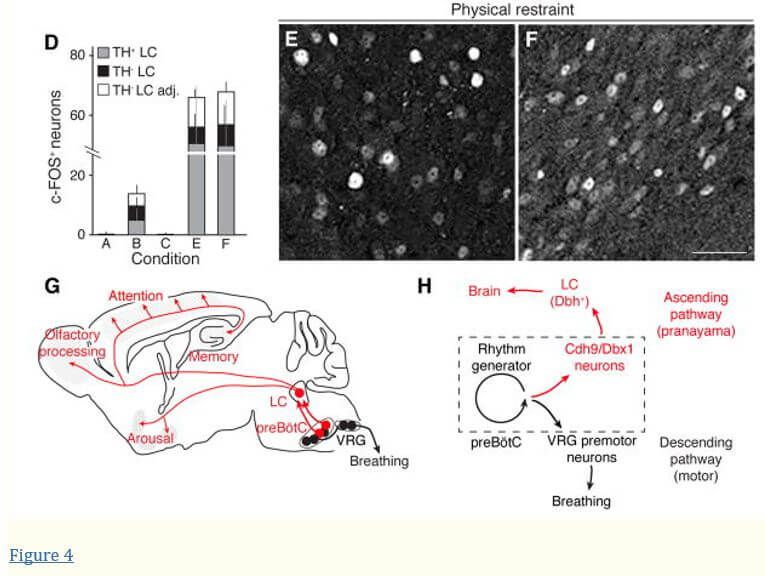
Nous avons examiné l’activité LC par l’expression de c-FOS ( 17 ) après l’ablation des neurones Cdh9/Dbx1. Dans des conditions de logement standard, les souris témoins Cdh9-LOSL-DTR;Dbx1-Cre avec des neurones Cdh9/Dbx1 intacts ont montré une activité LC occasionnelle (Figures 4A et D, et fig. S14 ). Lorsque les animaux ont été placés dans un nouvel environnement (chambre de pléthysmographie) pendant 1 heure, c-FOS a été induit dans des cellules dispersées tout au long du LC (Figures 4B et D, et fig. S14 ). Cependant, quatre jours après l’ablation des neurones Cdh9/Dbx1, seuls de rares neurones LC positifs au c-FOS ont été détectés avant ou après le placement dans la chambre (Figures 4C et D, et fig. S14 ). Le LC des animaux ayant subi une ablation est resté sensible au stimulus d’excitation extrême du stress de contention physique ( 18 ) (Fig. 4D à F, et fig. S13 ), indiquant que les autres entrées et fonctions LC étaient intactes.
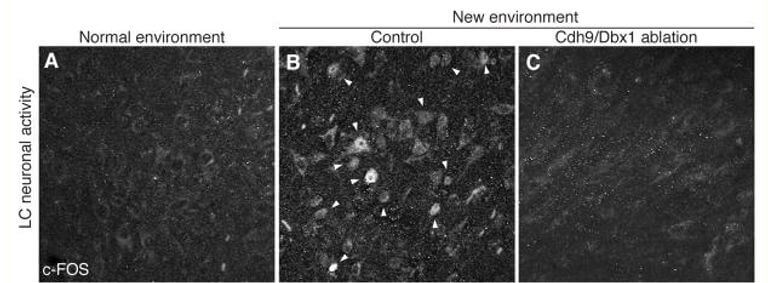
Effet de l’ablation des neurones Cdh9/Dbx1 sur l’activité neuronale LC
Immunomarquage A–C, E–F, c-FOS (têtes de flèches) en LC de souris adultes de type sauvage dans un environnement normal (cage domestique, A) et de contrôle (souris de type sauvage, Cdh9-LOSL-DTR ou Dbx1-Cre, B,E) et souris Cdh9/Dbx1-ablées (Cdh9-LOSL-DTR ; souris Dbx1-cre 2 jours après l’injection de DT, C,F) après 1 heure dans une nouvelle chambre (B,C) ou dans un tube conique sous conditions physiques retenue (E,F). Barre, 50 μm. D , Quantification des neurones c-FOS + dans A–C et E–F (moyenne ± SD) par coupe de 25 μm de LC : A, 0,4 ± 0,8 neurones (n = 39 coupes, 6 animaux) ; B, 13,8 ± 6,5 neurones (14 coupes, 4 animaux) ; C, 0,1 ± 0,3 neurones (17 coupes, 6 animaux) ; E, 61,4 ± 31,4 neurones (5 coupes, 3 animaux) ; F, 63,8,8 ± 19,9 neurones (6 coupes, 3 animaux). neurones c-FOS + /TH + , gris ; c-FOS+ /TH − neurones intégrés dans TH + , noir ; c-FOS + /TH – neurones entourant directement la région TH + LC, blanc. G, Circuit neuronal ascendant de preBötC. Les neurones Cdh9/Dbx1 preBötC (rouges) fournissent une entrée excitatrice monosynaptique aux neurones noradrénergiques du locus coeruleus (LC) (rouges), qui se projettent dans tout le cerveau pour favoriser l’éveil et les comportements actifs. Le circuit classique des neurones générateurs de rythme préBötC (noir) aux prémotoneurones du groupe respiratoire ventral (VRG, noir) est également illustré. H,Modèle de preBötC avec des neurones Cdh9/Dbx1 distincts mais régulés par les neurones générateurs de rythme. Cela fournit un signal corollaire respiratoire ascendant à LC sur le reste du cerveau, séparé du circuit moteur descendant classique. Par conséquent, lorsque la respiration s’accélère ou est autrement altérée, les neurones Cdh9/Dbx1 activent LC pour induire ou maintenir un état d’éveil. (Des circuits moins directs ou des événements en aval des neurones Cdh9/Dbx1 pourraient également contribuer à l’activation de LC, et parce que LC régule également les modalités sensorielles ( 27 , 28 ), des altérations sensorielles pourraient également contribuer aux comportements induits par LC. En outre, une contribution directe de Cdh9 /Dbx1 neurones à la génération du rythme respiratoire préBötC ne peut être exclu, car des mécanismes compensatoires peuvent les obscurcir.)
Nous avons identifié et caractérisé un nouveau sous-type neuronal dans le preBötC comprenant ~175 de ses ~3000 neurones. Les Cdh9/Dbx1 sont indispensables pour la génération du rythme respiratoire et favorisent plutôt une excitation comportementale généralisée. L’ablation de ces neurones a laissé intacts tous les principaux schémas respiratoires et régulations, mais a rendu les souris incroyablement calmes : leur activité et leurs profils ECoG sont passés d’un comportement exploratoire actif et de schémas d’ondes cérébrales à des comportements calmes tels que rester assis et se toiletter. Le traçage monosynaptique a démontré que ces neurones se projettent directement et se synapsent sur les neurones noradrénergiques du LC controlatéral, qui à leur tour se projettent dans tout le cerveau et contrôlent l’éveil généralisé et les transitions veille-sommeil ( 15). Les neurones preBötC Cdh9 / Dbx1 fournissent une entrée excitatrice au LC et semblent être l’entrée d’activation dominante dans des conditions d’excitation douce de placement dans une nouvelle chambre.
Nous proposons que les neurones préBötC Cdh9/Dbx1 fonctionnent comme des neurones passerelles reliant directement le préBötC au locus coeruleus, et à travers lui au reste du cerveau (Figure 4G). Ce circuit ascendant permet au centre respiratoire de communiquer directement avec et de contrôler les structures cérébrales d’ordre supérieur associées à l’excitation comportementale. L’entrée excitatrice du LC est vraisemblablement fournie par les schémas d’activité associés à l’inspiration observés des neurones Cdh9 / Dbx1, qui pourraient fournir une plus grande entrée excitatrice avec des fréquences respiratoires plus rapides et peut-être des schémas respiratoires anormaux (Figure 4H). Ce signal corollaire respiratoire servirait ainsi à coordonner l’état d’éveil de l’animal avec le schéma respiratoire, laissant l’animal calme et détendu lorsque la respiration est lente et régulière, mais favorisant (ou maintenant) l’éveil lorsque la respiration est rapide ou perturbée. Ce circuit et ce signal corollaire expliqueraient pourquoi des schémas respiratoires préBötC ont été observés dans le LC et d’autres structures d’activation réticulaires ( 19 – 21 ). Le LC peut augmenter la fréquence respiratoire ( 22 ), il peut donc également y avoir une boucle de rétroaction positive du LC vers les neurones Cdh9/Dbx1 preBötC.
Le circuit Cdh9/Dbx1 peut avoir évolué comme une réponse de défense directe et rapide, mobilisant l’animal face à une respiration rapide, irrégulière ou laborieuse. En effet, une respiration rapide ou erratique chez l’homme augmente la vigilance et peut provoquer de l’anxiété et même de la panique ( 3 ). De même, une activité pré-BötC accrue, une hyperventilation et des soupirs semblent induire une excitation pendant le sommeil ( 23 – 25 ). À l’inverse, la respiration lente et contrôlée est connue depuis longtemps par les praticiens du pranayama yoga pour induire la relaxation, et les approches associées se sont avérées utiles dans les syndromes d’anxiété et autres troubles de stress ( 1 , 2). Si le circuit Cdh9 / Dbx1 est conservé chez l’homme, il pourrait fournir une cible thérapeutique pour les troubles anxieux liés à la respiration et peut-être la prévention du syndrome de mort subite du nourrisson (SMSN), largement supposé résulter d’une réponse d’éveil inadéquate à l’asphyxie pendant le sommeil ( 24 ) . Fait intéressant, les attaques de panique déclenchées par des symptômes respiratoires réagissent uniquement à la clonidine, un agoniste α2-adrénergique qui fait taire la LC ( 26 ).
Bien que la respiration soit généralement considérée comme un comportement autonome, les fonctions cérébrales d’ordre supérieur peuvent exercer un contrôle exquis sur la respiration. Nos résultats montrent, à l’inverse, que le centre respiratoire a une influence directe et puissante sur les fonctions cérébrales d’ordre supérieur. Il sera donc important de cartographier l’ensemble des comportements et fonctions contrôlés par le centre respiratoire.
Remerciements
Nous remercions les Drs. Xiaoke Chen et Greg Nachtrab pour l’assistance et les réactifs pour l’injection d’AAV-Cre, Jamie Zeitzer pour l’assistance à l’analyse ECoG et les membres du laboratoire de Krasnow pour leurs commentaires utiles. Ce travail a été soutenu par le Howard Hughes Medical Institute (MAK et LL), les subventions des NIH HL70029 (JLF), HL40959 (JLF) et le programme de formation des scientifiques médicaux des NIH (KY). MAK et LL sont des chercheurs du Howard Hughes Medical Institute.
Notes de bas de page
KY a effectué un criblage in situ , généré et caractérisé le transgène Cdh9, caractérisé l’ablation neuronale Cdh9/Dbx1, effectué des injections de billes AAV-Cre, Fluorogold et rétrogrades, et des expériences c-Fos. LAS et LL ont fourni des réactifs pour la rage et les virus CAV-Cre injectés par LAS. KK et JLF ont fourni des réactifs pour et KK a effectué et analysé l’électrophysiologie des tranches. JMS et JRH ont fourni des réactifs pour et JMS a effectué et analysé l’enregistrement ECoG. KY a analysé toutes les données. KY et MAK ont conçu des expériences, interprété des données et rédigé le manuscrit. Tous les auteurs ont édité le manuscrit.
Les données sont conservées et stockées dans le laboratoire de Krasnow : Howard Hughes Medical Institute, Department of Biochemistry, Stanford University School of Medicine, Stanford CA 94305, USA
Références et notes
- Brown RP, Gerbarg PL. Yoga respiration, méditation et longévité. Ann NY Acad Sci. 2009 ; 1172: 54–62. [ PubMed ] [ Google Scholar ]
- Brown RP, Gerbarg PL. Sudarshan Kriya Yoga respiration dans le traitement du stress, de l’anxiété et de la dépression : partie II-applications cliniques et lignes directrices. J Altern Complément Med. 2005 ; 11: 711–717. [ PubMed ] [ Google Scholar ]
- Nardi E, Freire RC, Zin WA. Trouble panique et contrôle de la respiration. Respir Physiol Neurobiol. 2009 ; 167:133–143. [ PubMed ] [ Google Scholar ]
- Parshall MB, et al. Une déclaration officielle de la société thoracique américaine : mise à jour sur les mécanismes, l’évaluation et la gestion de la dyspnée. Suis J de Respir Crit Care Med. 2012 ; 185: 435–452. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Feldman JL, Del Negro CA, Gray PA. Comprendre le rythme de la respiration : si proche, mais si loin. Annu Rev Physiol. 2013 ; 75: 423–452. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Smith JC, Ellenberger HH, Ballanyi K, Richter DW, Feldman JL. Complexe pré-Bötzinger : une région du tronc cérébral qui peut générer le rythme respiratoire chez les mammifères. Science. 1991; 254:726–729. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Yackle K, Ezran C, Kam K, Krasnow MA.en préparation. [ Google Scholar]
- Bouvier J, et al. Les interneurones du cerveau postérieur et le guidage des axones sont essentiels à la respiration. Neurosciences naturelles. 2010 ; 13:1066–1074. [ PubMed ] [ Google Scholar ]
- Gray PA, et al. Origine développementale des neurones respiratoires du complexe preBotzinger. J Neurosci. 2010 ; 30:14883–14895. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Li P, et al. Le circuit de contrôle peptidergique pour le soupir. Nature. 2016 ; 530: 293–297. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Diez-Roux G, et al. Un atlas anatomique à haute résolution du transcriptome chez l’embryon de souris. PLoS Biol. 2011 ; 9:e1000582. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Picardo MC, Weragalaarachchi KT, Akins VT, Del Negro CA. Propriétés physiologiques et morphologiques des neurones respiratoires dérivés de Dbx1 dans le complexe pré-Bötzinger de souris néonatales. J Physiol. 2013 ; 591:2687–2703. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Pierani A, Moran-Rivard L, Sunshine MJ, Littman DR, Goulding M, Jessell TM. Contrôle du destin des interneurones dans la moelle épinière en développement par la protéine homéodomaine progénitrice Dbx1. Neurone. 2001 ; 29: 367–384. [ PubMed ] [ Google Scholar ]
- Wang X, et al. L’ablation au laser des neurones Dbx1 dans le complexe pré-Bötzinger arrête le rythme inspiratoire et altère la production motrice chez les souris néonatales. eLife. 2014 ; 3:e03427. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Berridge CW, Waterhouse BD. Le système locus coeruleus-noradrénergique : modulation de l’état comportemental et des processus cognitifs dépendants de l’état. Cerveau Rés Cerveau Rév.2003 ; 42 : 33–84. [ PubMed ] [ Google Scholar ]
- Wickersham R, et al. Restriction monosynaptique du traçage transsynaptique à partir de neurones uniques génétiquement ciblés. Neurone. 2007 ; 53: 639–647. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Sheng M, Greenberg ME. La régulation et la fonction de c-fos et d’autres gènes précoces immédiats dans le système nerveux. Neurone. 1990 ; 4: 477–485. [ PubMed ] [ Google Scholar ]
- McCall JG, et al. L’engagement de la CRH du système noradrénergique du locus coeruleus médie l’anxiété induite par le stress. Neurone. 2015 ; 87: 605–620. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Guyenet PG, Koshiya N, Huangfu D, Verberne AJ, Riley TA. Contrôle respiratoire central des neurones noradrénergiques pontiques A5 et A6. Suis J Physiol. 1993 ; 264:R1034–1044. [ PubMed ] [ Google Scholar ]
- Oyamada Y, Ballantyne D, Mückenhoff K, Scheid P. Potentiel membranaire modulé par la respiration et chimiosensibilité des neurones du locus coeruleus dans la moelle épinière du tronc cérébral in vitro du rat nouveau-né. J Physiol. 1998 ; 513:381–398. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Chen Z, Eldridge FL, Wagner PG. Déclenchement rythmique associé à la respiration des neurones du mésencéphale chez le chat : relation avec le niveau de commande respiratoire. J Physiol. 1991; 437:305–325. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Hilaire G, Viemari JC, Coulon P, Simonneau M, Bevengut M. Modulation du générateur de rythme respiratoire par les groupes noradrénergiques pontiques A5 et A6 chez les rongeurs. Resp Physiol Neurobiol. 2004 ; 143:187–197. [ PubMed ] [ Google Scholar ]
- Gleeson K, Zwillich CW. Stimulation par l’adénosine, ventilation et éveil du sommeil. Suis Rev Respir Dis. 1992 ; 145: 453–457. [ PubMed ] [ Google Scholar ]
- Kinney HC, Thach BT. Le syndrome de la mort subite du nourrisson. N Engl J Méd. 2009 ; 361:795–805. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Ramírez JM. Le rôle intégratif du soupir en psychologie, physiologie, pathologie et neurobiologie. Prog Cerveau Rés. 2014 ; 209:91–129. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Valença M, et al. Clonidine dans le sous-type de trouble panique respiratoire. Arq Neuropsiquiatr. 2004 ; 62: 396–398. [ PubMed ] [ Google Scholar ]
- Jiang M, Griff ER, Ennis M, Zimmer LA, Shipley MT. L’activation du locus coeruleus améliore les réponses des cellules mitrales du bulbe olfactif à une faible entrée nerveuse olfactive. J Neurosci. 1996 ; 16:6319–6329. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Hickey L, et al. L’optoactivation des neurones du locus coeruleus évoque des changements bidirectionnels dans la nociception thermique chez le rat. J Neurosci. 2014 ; 34:4148–4160. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Bielle F, et al. Origines multiples des cellules de Cajal-Retzius aux bords du pallidum en développement. Neurosciences naturelles. 2005 ; 8:1002–1012. [ PubMed ] [ Google Scholar ]
- Gong S, et al. Cibler la recombinase Cre sur des populations de neurones spécifiques avec des constructions de chromosomes artificiels bactériens. Journal des neurosciences. 2007 ; 27:9817–9823. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Shaner NC, et al. Protéines fluorescentes rouges, oranges et jaunes monomères améliorées dérivées de Discosoma sp. protéine fluorescente rouge. Nature Biotechnol. 2004 ; 22:1567–1572. [ PubMed ] [ Google Scholar ]
- Muzumdar MD, Tasic B, Miyamichi K, Li L, Luo L. Une souris reporter cre à double fluorescence globale. Genèse. 2007 ; 45:593–605. [ PubMed ] [ Google Scholar ]
- Saito M, et al. Ablation cellulaire conditionnelle et ciblée médiée par le récepteur de la toxine diphtérique chez des souris transgéniques. Nature Biotechnol. 2001 ; 19: 746–750. [ PubMed ] [ Google Scholar ]
- Osoegawa K, et al. Bibliothèques de chromosomes artificiels bactériens pour le séquençage et l’analyse fonctionnelle chez la souris. Recherche sur le génome. 2000 ; 10:116–128. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Schwarz LA, et al. Traçage viral-génétique de l’organisation entrée-sortie d’un circuit central de noradrénaline. Nature. 2015 ; 524: 88–92. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Osakada F, Callaway EM. Conception et génération de vecteurs recombinants du virus de la rage. Protocole Nat. 2013 ; 8:1583–1601. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Kremer EJ, Boutin S, Chillon M, Danos O. Canine adenovirus vectors: an alternative for adenovirus-mediated gene transfer. Journal de virologie. 2000 ; 74: 505–512. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Schoenenberger P, Gerosa D, Oertner TG. Contrôle temporel de l’induction génique précoce immédiate par la lumière. PLoS One. 2009 ; 4:e8185. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Luckman SM, Dyball RE, Leng G. L’induction de l’expression de c-fos dans les neurones magnocellulaires hypothalamiques nécessite une activation synaptique et pas simplement une activité de pointe accrue. Journal des neurosciences. 1994 ; 14:4825–4830. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Peng H, Bria A, Zhou Z, Iannello G, Long F. Visualisation et analyse extensibles d’images multidimensionnelles à l’aide de Vaa3D. Protocoles naturels. 2014 ; 9: 193–208. [ PubMed ] [ Google Scholar ]
- Kreuzer M, et al. La notation du sommeil a rendu facile un logiciel d’analyse du sommeil semi-automatisé et des outils de nouvelle notation manuelle pour la recherche fondamentale sur le sommeil chez la souris. MéthodesX. 2015 ; 24: 232–240. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Karasinski P, Stinus L, Robert C, Limoge A. Score veille-sommeil en temps réel chez le rat à l’aide d’un seul canal EEG. Dormir. 1994 ; 17: 113–119. [ PubMed ] [ Google Scholar ]
- Schofield BR. Traçage axonal rétrograde avec des marqueurs fluorescents. Curr Protocole Neurosci. 2008 ; Chapitre 1(Unité 1.17) [ PubMed ] [ Google Scholar ]
- Callaway EM, Luo L. Circuit monosynaptique traçant avec des virus de la rage à glycoprotéine supprimée. Journal des neurosciences. 2015 ; 35:8979–8985. [ Article PMC gratuit ] [ PubMed ] [ Google Scholar ]
- Kam K, Worrell JW, Janczewski WA, Cui Y, Feldman JL. Rythmes inspiratoires distincts et mécanismes générateurs de motifs dans le complexe preBötzinger. J Neurosci. 2013;(33):9235–9245. [ Article PMC gratuit] [ PubMed ] [ Google Scholar ]
- Hama H, et al. Échelle : une approche chimique pour l’imagerie par fluorescence et la reconstruction du cerveau de souris transparent. Neurosciences naturelles. 2011;(14):1481–1488. [ PubMed] [ Google Scholar ]
www.ncbi.nlm.nih.gov/pmc/articles/PMC5505554/ – consulté le 26 août 2023
